Passos largos contra o câncer
Num cenário marcado por avanços notáveis contra o câncer, pesquisas recentes têm revelado conquistas significativas em diversas frentes. Cientistas da Universidade da Califórnia, nos Estados Unidos, criaram uma abordagem capaz de controlar a proteína MYC, expressa pelo gene de mesmo nome, presente em cerca de 75% dos tumores, traçando caminhos para tratamentos revolucionários. Um ensaio sobre meduloblastomas aprofundou a compreensão desse tipo de câncer cerebral infantil, abrindo portas para abordagens mais específicas. Para especialistas, os avanços coletivos são essenciais.
Pesquisadores da Universidade da Califórnia Riverside (UCR) publicaram, recentemente, na revista Journal of the American Chemical Society, avanços promissores no tratamento do câncer ao controlar a MYC, uma proteína disforme que agrava a maioria dos casos de tumores em humanos. Em células saudáveis, a MYC orienta o processo de transcrição genética. No entanto, nas estruturas cancerígenas, ela se torna hiperativa e desregulada.
"MYC é menos um alimento para as células cancerígenas e mais um esteroide que promove o rápido crescimento do câncer", contou, em comunicado, Min Xue, professor associado de química da instituição e co-autor do ensaio.
Domando a proteína
A equipe acreditava que atenuar a hiperatividade da substância poderia ser a chave para controlar a patologia. Contudo, o desafio era domar a proteína, pois, ao contrário de outras, ela não tem uma estrutura definida. O artigo detalha a criação de um composto peptídico que se liga ao MYC e suprime sua atividade. Essa substância mostra uma interação resistente e específica, semelhante à força de um anticorpo.
Os pesquisadores, liderados por Xue, utilizaram nanopartículas lipídicas para entregar o peptídeo nas células. Uma vez dentro da célula, o peptídeo se conecta à MYC, alterando suas propriedades físicas e impedindo atividades de transcrição genética.
Olhar para o futuro
Atualmente, os cientistas buscam criar produtos que aprimorem a capacidade do peptídeo de penetrar nas estruturas. O laboratório tem se dedicado ainda a desenvolver ferramentas moleculares para elaborar remédios. "MYC é basicamente uma bola de aleatoriedade. Os pipelines de descoberta de medicamentos convencionais dependem de estruturas bem definidas, e isso não existe para o MYC", frisou Xue.
Daniel Musse Gomes, oncologista da Oncologia D'Or e membro do Instituto D'Or de Pesquisa, ressaltou que o composto criado por engenharia genética é inédito. "A princípio é muito bem programado e ele vai inibir esse gene da proteína MYC num lugar específico. Esse gene faz as células do câncer se multiplicarem e torna o ambiente mais propício para essas estruturas se desenvolverem, faz as células tumorais ficarem viciadas nele, precisam que esse gene esteja sempre ativo para elas continuarem crescendo."
Gomes pontuou que um dos grandes desafios na aplicação desse composto é garantir que ele vá exatamente no tumor. "Então, é importante garantir que ele vá exatamente nessas células defeituosas. Se ligue de modo forte, de modo rápido, que essas células não desenvolvam resistência."
Esperança para os pequenos
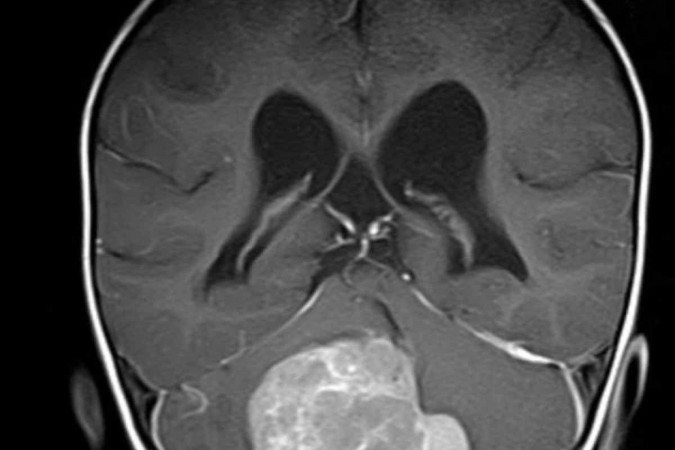
Para a equipe, os resultados do trabalho devem ajudar muitos pacientes. Ainda pensando em como personalizar os tratamentos de tumores, estudiosos de diferentes instituições alemãs conseguiram avanços na compreensão e tratamento de meduloblastomas, tumores cerebrais frequentes em crianças.
Utilizando uma técnica inovadora de análise de células, a equipe detalhou os programas genéticos dessas estruturas, identificando padrões de desenvolvimento no interior dos tumores. O estudo se concentrou em um subtipo chamado meduloblastoma com nodularidade extensa (MBEN), revelando que células cancerosas em certas áreas não se dividem ativamente, o que indica possibilidade de evolução mais benigna.
Baseados em características teciduais e critérios genéticos, os subtipos de meduloblastomas foram divididos em grupos de risco, delineando diferentes prognósticos e abordagens de tratamento. A descoberta de padrões nas células tumorais, especialmente em subtipos como MBEN, fornece uma base para explorar estratégias terapêuticas direcionadas, evitando tratamentos intensivos para crianças. O artigo destaca ainda a importância do bloqueio do processo de maturação como uma ferramenta potencial para direcionar as estruturas cancerígenas de volta a uma direção benigna.
Perto da solução
David Ghasem, médico, cientista de instituições alemãs e co-líder do estudo, afirma que o trabalho mostra que os MBENs estão mais próximos do desenvolvimento cerebelar normal do que se pensava antes. "Talvez as células apenas precisem de um pequeno 'impulso celular' na direção certa para se transformarem em estruturas cerebrais normais e não cancerosas. Essa forma de terapia, que não visa matar as células cancerígenas, mas sim reprogramá-las, poderia levar ao desenvolvimento de medicamentos menos tóxicos para as crianças que sofrem dessa terrível doença."
Sidnei Epelman, coordenador do Grupo Cooperativo de Meduloblastoma da Sociedade Brasileira de Oncologia Pediátrica (Sobope), detalhou que identificar qual o tipo de meduloblastoma é essencial. No Brasil, são oferecidos aos hospitais, que participam do projeto, a classificação molecular do tumor em subtipos para assim, apresentar o protocolo de tratamento específico. "A partir disso, sabemos de duas situações: qual é o risco maior desse paciente além dos outros fatores já conhecidos e o desenvolvimento de novas terapêuticas, se vai ser mais agressivo ou menos, e a melhor chance de cura."
Cientistas do Centro de Câncer Cedars-Sinai, nos Estados Unidos, realizaram uma grande análise das células de câncer de mama triplo-negativo, antes e após a radioterapia combinada com imunoterapia. O estudo, descrito na revista Cancer Cell, revelou três grupos distintos de pacientes com respostas variadas ao tratamento.
O câncer de mama triplo-negativo é notório pela sua agressividade, pacientes geralmente recebem tratamento pré-cirúrgico para reduzir tumores, quando a imunoterapia desempenha algum papel no combate à doença. Para o trabalho, os cientistas focaram na combinação de radioterapia e imunoterapia, analisando os tumores de 34 pessoas.
Os resultados destacaram a influência positiva da radioterapia na resposta imunológica, oferecendo visões importantes para o futuro de ensaios clínicos e abordagens específicas. Conforme o artigo, pacientes com esse tipo de tumor enfrentam desafios no tratamento, agora, os estudiosos confirmaram, que para algumas pessoas, a combinação avaliada pode desencadear uma resposta imunitária eficaz contra o tumor antes da cirurgia.
Para Simon Knott, cientista do Cedars-Sinai Cancer e autor sênior do estudo, a descoberta poderá evitar que pacientes sejam submetidos a abordagens muito incisivas, associadas a efeitos colaterais. "Isso poderia nos ajudar a empregar nossas opções de tratamento mais agressivas somente quando mais necessário", contou o cientista, em nota.
Elisa Porto, oncologista da Oncoclínicas Brasília, sublinha que as descobertas podem auxiliar na compreensão dos mecanismos da doença, na identificação de alvos terapêuticos e no desenvolvimento de abordagens de medicina personalizada. "Ao analisar os padrões de expressão gênica em resposta a diferentes tratamentos, poderemos avaliar sua eficácia, toxicidade, mecanismos de ação, prever respostas a drogas e otimizar a dosagem e combinações de estratégias."
Segundo a especialista, é consenso na comunidade científica que o câncer é uma doença heterogênea, o que explica a diferença das células cancerígenas entre pacientes e entre tumores da mesma pessoa. "O conceito de medicina de precisão tem revolucionado o campo da oncologia. Associando critérios clínico-patológicos com o perfil molecular, podemos criar estratégias de tratamento adaptadas às necessidades de cada pessoa."
Por que controlar essas proteínas?
É como se o DNA fosse o escritório de uma fábrica onde as decisões são tomadas, o RNA o mensageiro dessas decisões e as proteínas os operários que executassem as ordens. Se todo o processo acontecer em uma célula tumoral, cuja ordem final é fazer com que ela se divida, ao conseguir controlar as proteínas, a estrutura não poderá executar essa ação de divisão. Grande parte do avanço no tratamento do câncer vem do controle de proteínas presentes no tumor, via anticorpos monoclonais, que são proteínas injetadas nos pacientes e neutralizam aquelas produzidas pelo câncer.
Quais portas se abrem com essa descoberta?
O C-MYC tem sido apontado como peça central no processo carcinogênico e sua amplificação está relacionada com carcinomas invasivos que apresentam comportamento clínico mais agressivo e prognóstico reservado. O estudo conseguiu driblar a complexidade da estrutura MYC promover a inativação dessa proteína em um nível nunca atingido. Isso começa a lançar luz numa estratégia desejada dentro da oncologia, pois o C-MYC tem um papel central no aparecimento e desenvolvimento de vários tumores.
Utilizamos cookies próprios e de terceiros para o correto funcionamento e visualização do site pelo utilizador, bem como para a recolha de estatísticas sobre a sua utilização.
